眼刺激性試験法「Vitrigel®-EIT法」とは
眼刺激性試験法とは、化学物質が眼に付着することによって引き起こされる障害の重篤さを評価するための試験法です。従来はウサギの眼に被験物質を滴下して、障害の程度を観察する動物実験(ドレイズ試験)によって行われてきました。しかし、2013年にEUで化粧品に対する動物実験が禁止されたことを契機として、世界的に動物実験の実施を削減する流れが加速しています。このような社会状況を背景に、動物の代わりに培養細胞等を利用した各種の試験法(動物実験代替法)が開発されています。
人の眼で最も外界に近い組織が角膜です(図1)。角膜の表面にある上皮層は上皮バリア機能と呼ばれる機能を持っています。健康な状態では、化学物質や微生物等の異物が眼の表面に触れても、この上皮バリア機能が働いて眼の内部に侵入することはありません。一方、眼刺激性のある化学物質が眼に触れると、上皮バリア機能が破壊されて化学物質が角膜内部に侵入することで、角膜の浮腫や白濁等の障害が引き起こされます。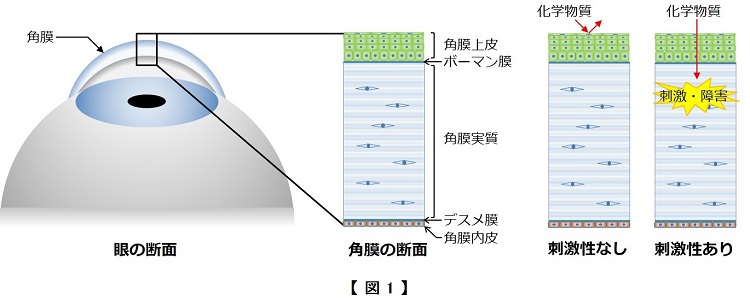
Vitrigel®-EIT法ではこの上皮バリア機能に着目しました。まず、ad-MEDビトリゲル®内で角膜上皮由来の細胞を培養することによって、上皮バリア機能と人の角膜上皮に類似した構造を持つ角膜上皮モデルを構築します(図2)。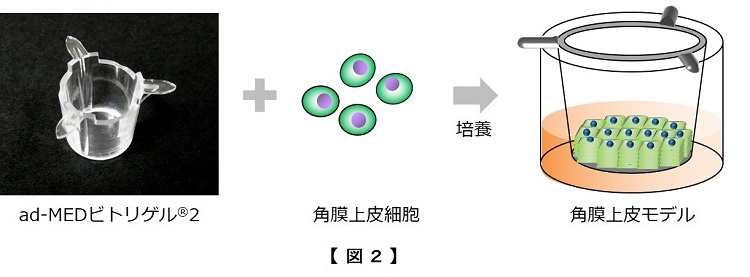
上皮バリア機能の健全性を簡便に評価する方法として、経上皮電気抵抗値(Transepithelial electrical resistance, TEER)測定があります。健全なバリア機能を有する組織が高いTEER値を示すのに対して、バリア機能が障害を受けるとTEER値は低下します。Vitrigel®-EIT法では、角膜上皮モデルに化学物質を滴下して、そのTEER値の変化を専用の測定装置で測定することで、わずか3分間で化学物質の眼刺激性の有無を判定することができます(図3)。
本試験法は2019年6月に国際的な公定法であるOECDテストガイドライン*No.494として収載されました。これによって世界各国で化粧品等の安全性試験に広く利用されることが期待されています。 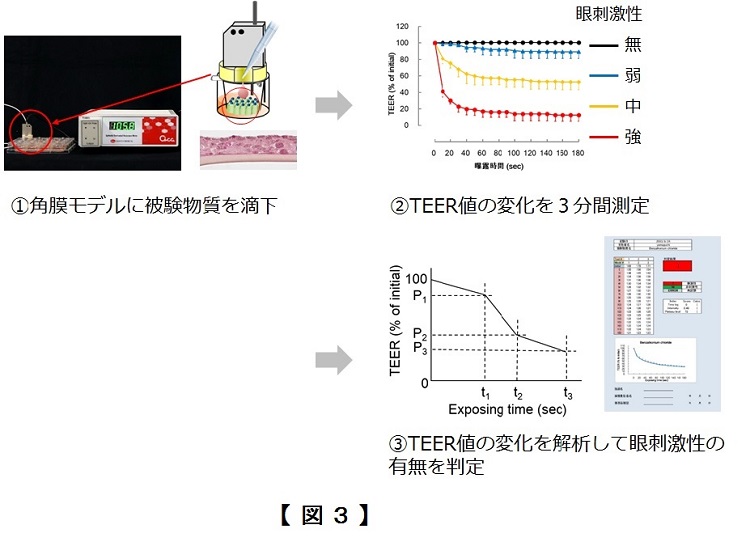
*「ビトリゲル®」、「Vitrigel®」について
「ビトリゲル®」、「Vitrigel®」は国立研究開発法人 農業・食品産業技術総合研究機構(農研機構)による登録商標です。眼刺激性試験法「Vitrigel®-EIT法」は、農林水産省「アグリ・ヘルス実用化研究促進プロジェクト」の支援を受けて、農研機構と共同で開発されました。
*OECDテストガイドラインとは
化学物質が人の健康や生態系へ及ぼす影響等を国際的に共通の方法で評価することを目的として経済協力開発機構(OECD)が収載した試験法のリストです。複数施設によるバリデーション試験や専門家による第三者評価によって有効性や信頼性を認められた試験法がOECDの審査を経てテストガイドラインに収載されます。
Vitrigel-EIT 法(動画)
この度、農研機構NAROチャンネルで、Vitrigel®-EIT法の紹介動画が公開されましたので、下記のリンクにてご紹介させて頂きます。
※上記動画については農研機構より了承を得て掲載しております。許可なく転載することを禁じます。
※農研機構の事情等により、予告なく動画のリンクが切れる場合がございます。ご了承ください。
製品情報
関連リンク
- 農研機構NAROチャンネル;Vitrigel-EIT (Eye Irritancy Test) 法(動画)
- 農研機構 プレスリリース(2019年7月5日);Vitrigel®-EIT法がOECDテストガイドラインに収載
- 農研機構 プレスリリース(2021年8月17日);改訂Vitrigel®-EIT法がOECDテストガイドラインに収載
- OECDテストガイドラインNo.494
- 日本動物実験代替法評価センター(JaCVAM) HP
研究発表
論文
- Multi-laboratory Validation Study of the Vitrigel-Eye Irritancy Test Method as an Alternative to In Vivo Eye Irritation Testing
H.Kojima, H.Yamaguchi, T.Sozu, N.Kleinstreuer, L.Chae-Hyung, W.Chen, M.Watanabe, T.Fukuda, K.Yamashita, T.Takezawa
Alternatives to Laboratory Animals, 47(3-4),140-157(2019).
- コラーゲンビトリゲル膜チャンバーを用いた眼刺激性試験法
竹澤俊明、山口宏之
皮膚の安全性・有用性評価法、㈱技術情報協会、73-77(2018).
- Predictive performance of the Vitrigel-eye irritancy test method using 118 chemicals
H. Yamaguchi, H. Kojima, T. Takezawa
Journal of Applied Toxicology, 36(8), 1025-1037 (2016).
- ad-MEDビトリゲル®とその創薬,化学物質安全性試験への応用
山口宏之
THE CHEMICAL TIMES, 241, 22-27 (2016).
- Vitrigel-eye irritancy test method using HCE-T cells
H. Yamaguchi, H. Kojima, T.Takezawa
Toxicological Sciences, 135(2), 347-355(2013).
- Development of a human corneal epithelium model utilizing a collagen vitrigel membrane and the changes of its barrier function induced by exposing eye irritant chemicals
T.Takezawa, K.Nishikawa, Pi-Chao.Wang
Toxicology in Vitro, 25(6), 1237-1241(2011).
外部発表
- 固体を含む被験物質に使用可能なVitrigel-EIT法の改訂手順の提案
山口宏之、押方歩、綿谷弘勝、小島肇、竹澤俊明
日本動物実験代替法学会第33回大会、2020年
- Vitrigel-EIT法を固体に適用するための新たな適用範囲の提案
山口宏之、押方歩、綿谷弘勝、小嶋肇、竹澤俊明
日本動物実験代替法学会第32回大会、2019年
その他のアプリケーション開発
ad-MEDビトリゲル®、ad-MEDビトリゲル®2を用いた臓器モデル開発について発表された文献、当社が参加した外部発表を紹介します。
論文
iPS細胞からの小腸モデル作製
- Generation of human-induced pluripotent stem cell-derived functional enterocyte-like cells for pharmacokinetic studies
S.Yoshida, T.Honjo, K.Iino, R.Ishibe, S.Leo, T.Shimada, T.Watanabe, M.Ishikawa, K.Maeda, H.Kusuhara, N.Shiraki, S.Kume
Stem Cell Reports, Vol.16, 1–14(2021).
iPS細胞からの肝臓モデル作製
- Collagen vitrigel promotes hepatocytic differentiation of induced pluripotent stem cells into functional hepatocyte-like cells
S.Nakai, I.Shibata, T.Shitamichi, H.Yamaguchi, N.Takagi, T.Inoue,T.Nakagawa, J.Kiyokawa, S.Wakabayashi, T.Miyoshi, E.Higashi, S.Ishida, N.Shiraki, S.Kume
Biology Open, 8(7), bio042192(2019).
肝臓モデル作製
- Prediction of Human Hepatic Clearance for Cytochrome P450 Substrates via a New Culture Method Using the Collagen Vitrigel Membrane Chamber and Fresh Hepatocytes Isolated from Liver Humanized Mice
R.Watari, M.Kakiki, C.Yamasaki, Y.Ishida, C.Tateno, Y.Kuroda, S.Ishida, K.Kusano
Biological and Pharmaceutical Bulletin, 42(3), 348-353(2019).
- A long-term culture system based on a collagen vitrigel membrane chamber that supports liver-specific functions of hepatocytes isolated from mice with humanized livers
R.Watari, M.Kakiki, A.Oshikata, T.Takezawa, C.Yamasaki, Y.Ishida, C.Tateno, Y.Kuroda, S.Ishida, K.Kusano
The Journal of Toxicological Sciences, 43(8), 521-529(2018).
- Development of an oxygenation culture method for activating the liver-specific functions of HepG2 cells utilizing a collagen vitrigel membrane chamber
A.Oshikata-Miyazaki, T.Takezawa
Cytotechnology, 68(5), 1801-1811(2016).
薬剤の角膜透過性試験
- Fabrication of a Corneal Model Composed of Corneal Epithelial and Endothelial Cells via a Collagen Vitrigel Membrane Functioned as an Acellular Stroma and Its Application to the Corneal Permeability Test of Chemicals
H.Yamaguchi, T.Takezawa
Drug Metabolism and Disposition, 46(11), 1684-1691(2018).
皮膚感作性試験
- Development of a Novel in Vitro Skin Sensitization Test Method using a Collagen Vitrigel Membrane Chamber
H.Miyazaki, K.Yamashita, T.Uchino, T.Takezawa, H.Kojima
Alternatives to Animal Testing and Experimentation, 22(2), 347-355(2017).
外部発表
iPS細胞からの肝臓または小腸モデル作製
- メチオニン除去培地とコラーゲンビトリゲル薄膜を用いて分化誘導したヒトiPS細胞由来肝臓細胞を利用した薬物毒性試験系の構築
柴田伊真、下道隆広、渡邊輝彦、山口宏之、白木伸明、粂昭苑
細胞アッセイ研究会シンポジウム「細胞アッセイ技術の現状と将来」、2019年
- ヒトiPS細胞から機能的な小腸上皮吸収細胞への新規分化誘導系の構築
本荘貴之、飯生啓太、前田和哉、渡邊輝彦、石川晶也、楠原洋行、白木伸明、粂昭苑
第41回日本分子生物学会年会、2018年
- ヒトiPS細胞から肝臓細胞への新規分化誘導系の構築、および初代培養肝細胞との機能比較
仲井峻、山口宏之、高木信幸、井上智彰、中川俊人、清川順平、白木伸明、粂昭苑
2017年度生命科学系学会合同年次大会、2017年